平成28年3月7日に第十七改正の日本薬局方が公示されました。第十七改正日本薬局方*では新たに精製ヒアルロン酸ナトリウム点眼液が追加されています。薬局方に準拠した精製ヒアルロン酸ナトリウム点眼液の定量分析ではシステム適合性としてヒアルロン酸とイプシロン-アミノカプロン酸の分離度(Rs)は5以上、システム再現性として6回の繰り返し分析においてヒアルロン酸のピーク面積の相対標準偏差は2.0 %以下となっています。OHpak SB-802.5 HQを用いて分析を行ったところ、システム適合性、システム再現性共に条件を満たすことが確認できました。
*データ採取時の版
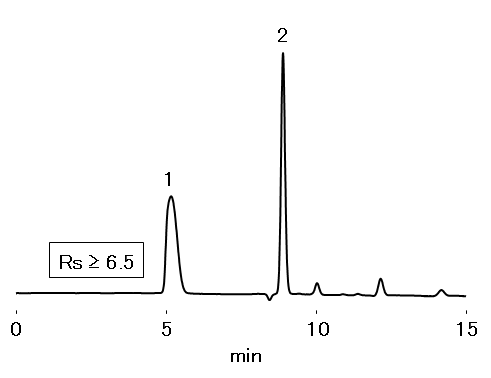
Sample : 20 μL
System suitability solution (prepared according to JP method)
1. Hyaluronic acid
2. ε-Aminocaproic acid
Column : Shodex OHpak SB-802.5 HQ (8.0 mm I.D. x 300 mm) Eluent : 0.1 M Na2SO4 aq. Flow rate : 1.0 mL/min Detector : UV (210 nm) Column temp. : 40 ℃
試料名インデックス
製品名インデックス
アプリケーションデータ
- EPに準拠したエリスロポエチンの分析 (LW-803)
- EPに準拠したソマトロピンの分析 (LW-803)
- EPに準拠したテリパラチドの分析 (KW-802.5)
- USP-NFに準拠したEthylcellulose Dispersion Type Bの分析 (KF-802)
- USP-NFに準拠したアジスロマイシンの分析 (ODP-50 4E)
- USP-NFに準拠したアジスロマイシン注射液の分析 (ODP-50 4D)
- USP-NFに準拠したアスコルビン酸注射液の分析 (DM-614)
- USP-NFに準拠したアラニンおよびアスパラギン酸の類縁物質分析 (SH1011)
- USP-NF GENERAL CHAPTERS「インスリンの物理化学的分析手順」の高分子タンパク質分析 (KW-802.5)
- USP-NFに準拠したエキセナチドの分析 (KW-802.5)
- USP-NFに準拠したエポエチンの分析 (LW-803)
- USP-NFに準拠したオメガ3脂肪酸のオリゴマー分析 (KF-802.5 + KF-802 + KF801)
- USP-NFに準拠したキシリトールの分析 (SP0810)
- USP-NFに準拠したグアーガムの分析 (SP0810)
- USP-NFに準拠したクランベリージュース中の混入物スクロースとソルビトールの分析 (SC1011-7F)
- USP-NFに準拠したザナミビルの分析 (NH2P-50 4E)
- USP-NFに準拠したセフェピム注射液中のN-メチルピロリジン分析 (YK-421)
- USP-NFに準拠したソルビトールの分析 (SP0810 8C)
- USP-NFに準拠したタガトースの定量分析 (SC1011)
- USP-NFに準拠したデキストロースの分析 (SC1011)
- USP-NFに準拠したトレハロースの分析 (KS-801)
- USP-NFに準拠したパミドロン酸二ナトリウムの分析 (I-524A)
- USP-NFに準拠したベタデックススルホブチルエーテルナトリウムの分析 (SB-803 HQ)
- USP-NFに準拠したポリエチレングリコール3350の重量平均分子量と分散度の測定 (SB-803 HQ)
- USP-NFに準拠したポリエチレングリコール3350の定量分析 (SB-802.5 HQ)
- USP-NFに準拠した内用液用ポリエチレングリコール3350の定量分析 (SB-802.5 HQ)
- USP-NFに準拠したボリコナゾールの不純物分析 (CDBS-453)
- USP-NFに準拠したマルチトールの分析 (SP0810 8C)
- USP-NFに準拠したマルトースの分析 (KS-801)
- USP-NFに準拠したモノカプリル酸プロピレングリコールの分析 (KF-801)
- USP-NFに準拠したラミブジンの不純物分析 (CDBS-453)
- USP-NFに準拠したリボースの分析 (KS-801)
- USP-NFに準拠した酢酸カルシウムカプセルの分析 (YK-421)
- USP-NFに準拠した硫酸亜鉛配合剤注射液の分析 (YK-421)
- USP-NFの薬局方フォーラムで提案されているイバンドロン酸ナトリウムの分析 (I-524A)
- USP-NFの薬局方フォーラムで提案されているエピネフリン注射液の分析 (CDBS-453)
- USP-NFの薬局方フォーラムで提案されているスクロースの分析 (SC1011-7F)
- USP-NFの薬局方フォーラムで提案されているフルオロウラシル注射液の不純物である尿素の分析 (SB-802.5 HQ)
- USP-NFの薬局方フォーラムで提案されているマンニトール注射液の分析 (SP0810)
- USP-NFに準拠した内服液用炭酸水素カリウム・塩化カリウム発泡錠のカリウム分析 (YK-421)
- USP-NFに準拠した内服液用炭酸水素ナトリウム・炭酸水素カリウム・クエン酸発泡錠の炭酸水素ナトリウムと炭酸水素カリウムの定量分析 (YK-421)
- USPに準拠したステアリン酸グリセリルの分析 (KF-802)
- USPに準拠したジステアリン酸グリセリルの分析 (KF-802)
- USPに準拠したトリステアリン酸グリセリルの分析 (KF-802)
- USP-NF GENERAL CHAPTERS <209> に準拠した低分子量ヘパリンの分子量測定 (KW-803 + KW-802.5)
- 日本薬局方に準拠したアジスロマイシンの分析 (ODP-50 4E)
- 日本薬局方に準拠したアレンドロン酸ナトリウム水和物の定量 (DS-413)
- 日本薬局方に準拠したアレンドロン酸ナトリウム水和物の類縁物質の分析 (DS-413)
- 日本薬局方に準拠したアレンドロン酸ナトリウム注射液の定量 (DS-613)
- 日本薬局方に準拠したアレンドロン酸ナトリウム錠の定量 (DS-613)
- 日本薬局方に準拠したインスリン グラルギンの分析 (KW-802.5)
- 日本薬局方に準拠したトレハロースの分析 (KS-801)
- 日本薬局方に準拠したヒトインスリンの分析 (KW-802.5)
- 日本薬局方に準拠したボグリボースの分析 (NH2P-50 4E)
- 日本薬局方に準拠したマルトース水和物の分析 (KS-801)
- 日本薬局方に準拠したミグリトールの分析 (NH2P-50 4E)
- 日本薬局方に準拠したラクツロースの分析 (SP0810)
- 薬局方に準拠したインスリン アスパルト中の高分子不純物の分析 (KW-802.5)
- 薬局方に準拠したポビドン中のギ酸分析 (KC-811)
- 薬局方に準拠したホルモテロール フマレート二水和物の分析 (ODP-50 4D)
- 薬局方に準拠したマンニトールの分析 (SC1011-7F)
