9. 分離モードの種類
HPLCカラムを選択する際、試料中に分析種の種類が少なく夾雑物もほとんど存在しない試料であれば、分析種がカラムから溶出さえすれば良く、カラム選択の幅は広いですが、試料中に分析種や夾雑物が複数存在する場合は、分析種がカラムから溶出することはもちろんのこと、分析種同士または夾雑物と分離できるカラムを選ぶ必要があります。そこでカラム選択の第一歩は、「どの分離モードを選択するか」です。「5. 分離の原理」では「相互作用の程度が異なれば分離ができる」と説明しましたが、このことは「分析種同士または夾雑物との性質の差を利用すれば分離できる」と言い換えることができます。各分離モードで利用する性質の違いを表1にまとめました。
(表1)分離モードで利用する性質の違い
| 分離モード | 性質の違い |
|---|---|
| 逆相、順相、親水性相互作用 (HILIC) | 極性 |
| イオン交換、イオン排除 | イオン性 |
| 配位子交換 | 配位子交換能 |
| サイズ排除 (SEC) | 分子サイズ(分子量) |
| 光学分割、アフィニティー | 特異性 |
| マルチモード | 性質の差の組み合わせ |
ここからは、各分離モードの分離機構を説明します。
10. 極性の差で分離
最初に極性の差を利用した分離モードについて説明します。 物質の極性を示す表現として高極性、低極性などを用いますが、同じ意味合いで親水性や疎水性という表現もしばしば使われます。親水性は水に溶け易さを示し、疎水性は水への溶けにくさを示します。「極性が高い」=「親水性が高い」、「極性が低い」=「疎水性が高い」と言い換えられます。
10-1. 逆相モード(逆相クロマトグラフィー)の分離機構
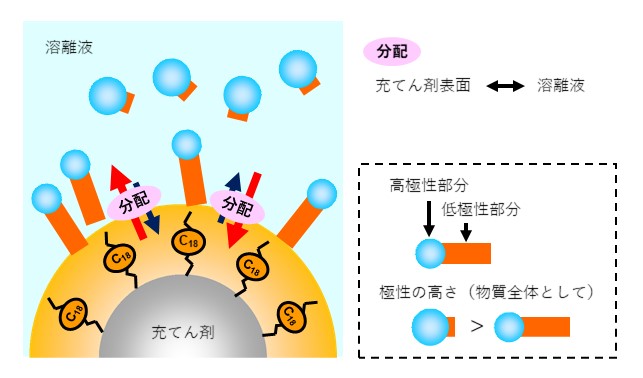
逆相モードは分析種の極性の差を利用した分離モードで、HPLC全体の80%以上が逆相モードを使用すると言われており、最も多用されている分離モードです。逆相モードでは、表面の極性が低い充てん剤と高極性溶媒(水/アセトニトリル、水/メタノールなどの混合溶液)の溶離液を用います。分析種は、「充てん剤の極性」<「溶離液の極性」の環境下で分配されます。このため、極性の高い分析種ほど溶離液側への分配が大きい、すなわちカラム内での移動速度が速いためカラムから早く溶出します。一方、分析種の極性が低いものは充てん剤側への分配が大きいためカラムからの溶出は遅れます。このように逆相モードでは基本的に極性の高い分析種の順番に溶出します。
図14に逆相モードの分離機構を、図15に逆相モードによるアルキルアルコールの溶出順序を示します。アルキル鎖(赤字)が大きいアルコールほど溶出が遅くなることが分かります。
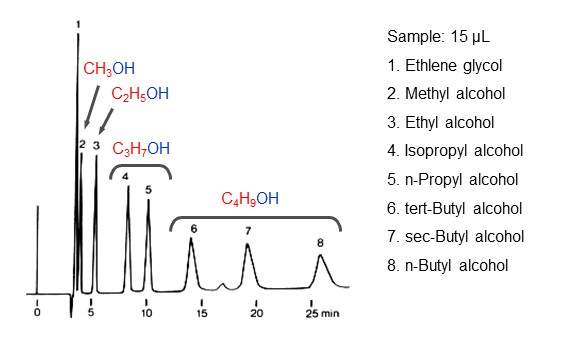
- Column
- : Shodex RSpak DE-613 (6.0 mm I.D. x 150 mm)
- Eluent
- :H2O
- Flow rate
- :1.0 mL/min
- Detector
- :RI
- Column tamp.
- :60 ℃
ODSカラム
逆相モード用カラムの代表格はODSカラムです。下記のように炭素数が18の直鎖アルキル基(オクタデシル基)がシリカ基材の表面に結合した充てん剤が充てんされています。オクタデシル基をシリカ基材に結合する時は、オクタデシルシラン化合物をシリカ基材表面にあるシラノール基に反応(シリル化)させるため、オクタデシルシリル (Octadecylsilyl)が結合したカラムということでODSカラムと名付けらました。シリカ基材の中ではODSカラムの割合は圧倒的に多く、HPLC全体で最も多く使用されているカラムと言っても過言ではありません。
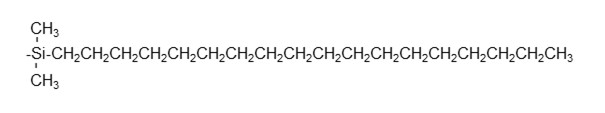
エンドキャッピング
シリカ基材に官能基を結合させる際、すべてのシラノール基に官能基が結合するわけではなく、一部のシラノール基はシリル化されずに残ります。この反応せずに残ったシラノール基を残存シラノール基と言います。残存シラノール基は分析種によっては意図しない二次的な相互作用を引き起こし、分離に影響を与えることがあります。通常は残存シラノール基にエンドキャッピングと呼ばれる二次シリル化の処理を行い二次的な相互作用が起きないようにするのですが、エンドキャッピングを行っても完全にシラノール基をシリル化させることは難しいと言われています。ODSカラムであっても使用するカラムによって分析結果が異なることがあるのは残存シラノール基が原因の1つです。ここでは、説明を割愛しますが、ODSカラムには結合様式にモノメリック型とポリメリック型があり、この違いによっても分離特性が変わると言われています。
参照:ODSとシラノール
その他のシリカ系逆相モード用カラム
逆相モード用カラムの中ではODSカラムが最も一般的ですが、オクタデシル (C18)基では分析種の保持が強すぎる場合は直鎖アルキル基の炭素数を短くした官能基に変更することで保持を弱めることが可能となります。以下に一例を示します。
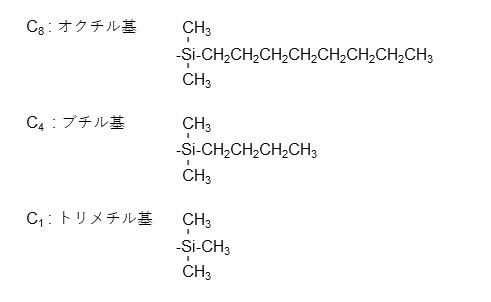
この他にフェニル基、シアノプロピル基などが結合された逆相カラムもあります。
ポリマー系逆相モード用カラム
逆相モード用カラムには充てん剤にポリマー基材を用いたものもあります。ポリマー系逆相モード用カラムの主な特長以下の通りです。
- (1)耐久性
シリカ系基材の充てん剤は使用中や保管中に加水分解を受け、官能基が外れるという現象がしばしば起こります。一方、ポリマー系基材は化学的な結合安定性が高く、カラムの耐久性が高いと言われています。 - (2)再現性
シリカ基材の充てん剤は製造ロット毎の品質管理が難しいですが、ポリマー基材はシリカ基材と比べて製造工程をコントロールしやすく、安定した品質を維持できます。
参照:RSpak DEシリーズの特長 (4) (ロット再現性) - (3)アルカリ耐久性
一般的にシリカ基材はアルカリ耐久性が低いと言われています。塩基性化合物の分析では、溶離液にアルカリ性の溶媒を使用することがあるため、アルカリ耐久性の高いポリマー基材が有効です。また、充てん剤に不純物が吸着してカラムの分離性能が低下した時にアルカリ洗浄が有効な場合があります。シリカ基材の充てん剤はアルカリ洗浄できずにカラム交換を余儀なくされる場合でも、ポリマー基材の充てん剤ならばアルカリ洗浄が行えるため、再生の可能性が高まります。
参照:ポリマー系逆相クロマトグラフィー用カラムODP-50 4Eのアルカリ条件下での繰り返し再現性
ODP2 HPの特長 (5) (アルカリ耐久性) - (4)分離性能
一般的にシリカカラムに比べてポリマーカラムの分離性能はやや劣るといわれていますが、ポリマーカラムも日々性能が向上しています。
Shodexは、長年培った高分子合成技術を活かし、様々なポリマー系逆相カラムを開発しています。その中でも最も使用されているのはAsahipak ODPシリーズです。オクタデシル基 (Octadecyl)が結合したポリマー (Polymer)基材(ポリビニルアルコールゲル)ということでODPと名付けました。ODSカラムに馴染みのあるユーザーにもイメージしやすいと思います。
Shodexのポリマー系逆相モード用カラムには、ポリマー基材自体の極性の低さを活かし、官能基導入しない基材のみの充てん剤を用いた製品を複数ラインアップしています。それぞれ充てん剤表面の極性やポアサイズが異なります。
10-2. 順相モード(順相クロマトグラフィー)の分離機構
次に順相モードについて説明します。順相モードも逆相モードと同じように分析種の極性の差を利用した分離モードです。順相モードでは、表面の極性が高い充てん剤(シリカゲル単体など)と非極性溶媒(ヘキサンとイソプロピルアルコールなどの混合溶液)の溶離液を用います。分析種は、「充てん剤表面の極性」>「溶離液の極性」の環境下で吸着(または分配)が起こります。逆相モードとは逆に極性の低い分析種の方がカラム内での移動速度が速くなるため、順相モードでは基本的に極性の低い分析種の順番に溶出します。
10-3. HILICモード(親水性相互作用クロマトグラフィー)の分離機構
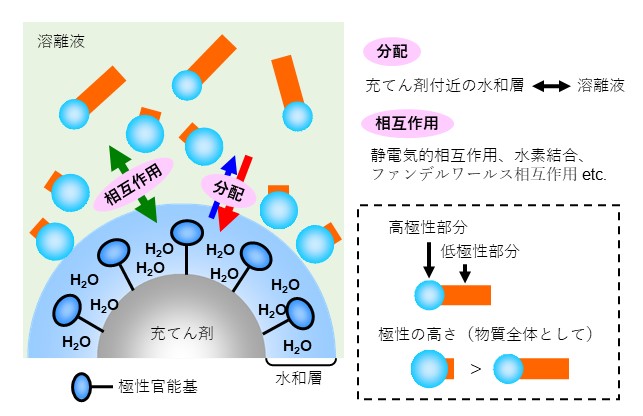
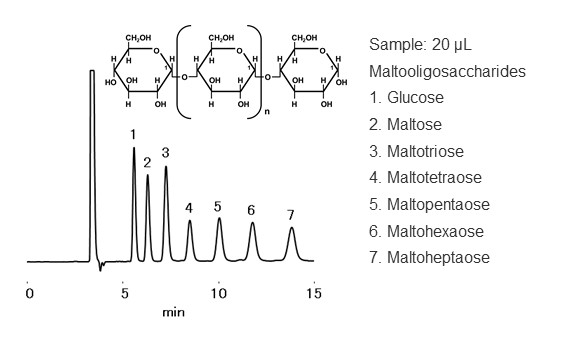
HILIC(ヒリック)とは、親水性相互作用クロマトグラフィー (Hydrophilic Interaction Liquid Chromatography)の略称で、1990年にアメリカのA. J. Alpertによって提唱されました。HILICモードは、広義には順相モードに属し、糖分析などは1990年以前から順相モードとして利用されていた歴史的な背景があります。HILICモードでは、シリカやポリマー基材にアミド基やアミノ基、ジオール基などの官能基が結合した表面の極性が高い充てん剤を使用します。溶離液は逆相モードと同様、水とアセトニトリル混合溶液など高極性溶媒を用いますが、HILICモードでは高い有機溶媒比率で使用します。この環境下では、充てん剤の表面に水和層が形成され、分析種は「充てん剤表面の極性」>「溶離液の極性」の環境下で分配され、極性の高い分析種の順番に溶出します。HILICモードは、溶離液は逆相モードと類似していても溶出順序は逆相モードの逆と覚えておくと良いかもしれません。HILICモードは、分配以外に静電的相互作用や水素結合、ファンデルワールス相互作用なども複合的に働きます。図16にHILICモードの分離機構を、図17にHILICモードによるマルトオリゴ糖の溶出順序を示します。マルトオリゴ糖はグルコースがα-1,4 グルコシド結合したオリゴ糖です。グルコースは構造内に水酸基 (OH基)が複数あり、結合するグルコースの数が多くなるほど極性が高くなります。糖鎖が大きいオリゴ糖ほど溶出が遅いことが分かります。
- Column
- :Shodex HILICpak VG-50 4E (4.6 mm I.D. x 250 mm)
- Eluent
- :CH3CN/H2O=65/35
- Flow rate
- :0.7 mL/min
- Detector
- :RI
- Column tamp.
- :40 ℃
HILICモードは、逆相モードでは保持が弱いまたは保持しにくい高極性化合物を分析することが可能です。この特長を活かし、HILICモードは糖分析を始めとして様々な高極性化合物の分析に用いられます。Shodexでは、ポリマー基材にアミノ基を結合した充てん剤を充てんしたAsahipak NH2Pシリーズカラムの他、ポリマー基材に様々な官能基を結合させたHILICpakシリーズをラインアップしています。これらのHILICモード用カラムは、ポリマー系逆相モード用カラムと同様、化学的な結合安定性が高く、アルカリ耐久性にも優れています。
逆相モード、順相モード、HILICモードの比較を表2にまとめました。
(表2)逆相モード、順相モード、HILICモードの比較
| 分離モード | 逆相モード | 順相モード | HILICモード |
|---|---|---|---|
| 充てん剤表面 | 低極性 | 高極性 | 高極性 |
| 溶離液 | 高極性 | 低極性 | 高極性 |
| 分析種の溶出順序 | 極性が高い順に溶出 | 極性が低い順に溶出 | 極性が高い順に溶出 |
| 対象試料 | 薬物、界面活性剤、ペプチド、水溶性ビタミンなど | 脂肪酸、リン脂質、脂溶性ビタミンなど | 糖、オリゴ核酸、アミノ酸、ペプチド、医薬品代謝物など |
| 特徴 | ・主に低分子(分子量2,000以下)が対象 ・幅広い試料に適用が可能 |
・主に低分子(分子量2,000以下)が対象 ・逆相で保持が強すぎる化合物に好適 ・立体構造認識能が高く、異性体分離に好適 ・溶離液の除去が簡易で分取・濃縮がしやすい |
・主に低分子(分子量2,000以下)が対象 ・逆相モードでは保持しづらい高極性化合物に好適 ・高極性化合物のLC/MSによる微量分析(高感度分析)に好適 |
Shodexの逆相モード用カラム、HILICモード用カラムはこちら
11. イオン性の差で分離
磁石のN極とS極が引きつけ合うように正の電荷を帯びた「陽イオン」と負の電荷を帯びた「陰イオン」は引きつけ合います。一方、N極同士やS極同士のように陽イオン同士、陰イオン同士は反発し合います。イオン性物質には、タンパク質やペプチド、アミノ酸、カテコールアミンなどの生体物質や有機酸などの有機物の他、塩化物イオン (Cl-)やナトリウムイオン (Na+)などのような無機イオンなど様々なものがあります。ここでは、イオンの引き合う力(静電的相互作用)を利用したイオン交換モードとイオン同士が反発し合う力(静電的反発)を利用したイオン排除モードについて紹介します。
11-1. イオン交換モード(イオン交換クロマトグラフィー)の分離機構
ここでは、分析種が陰イオン物質の場合を例にイオン交換モードの分離機構を説明します。 分析種が陰イオン物質の場合は、充てん剤には陽イオン官能基を使用します。イオン交換モードでは、一般的に緩衝液や塩の水溶液を溶離液に用います。
- 溶離液中の陰イオンは静電的相互作用で官能基の陽イオンに吸着します。溶離液は連続的にカラムを通過するため溶離液中の陰イオン同士で競合し、吸脱着を繰り返しながらカラム内を移動します。(図18の(1))
- 分析種(陰イオン物質)がカラムに導入されると分析種は吸着していた溶離液由来の陰イオンと競合し、官能基に吸着します。(図18の(2)、(3))
- 分析種は溶離液中の陰イオンと競合しながら(脱離と吸着を繰り返しながら)カラムの中を移動します。(図18の(4)、(5))
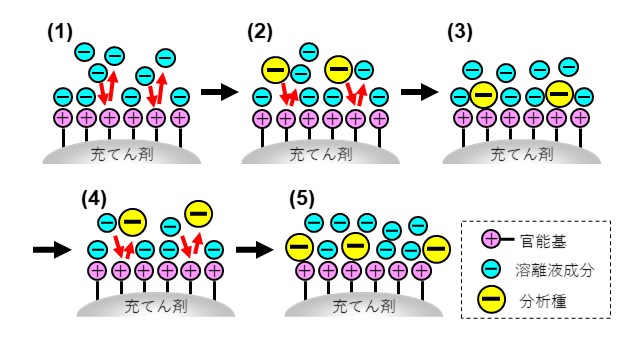
分析種は溶離液中の競合イオンと交換しながらカラム内を移動することから溶離液のイオン強度が高くなると分析種の保持が弱まります。イオン交換モードでは、保持が強い分析種を早く溶出させるために経時的に溶離液の組成を変化させる「グラジエント溶出」を行うことが一般的です。代表的なグラジエント溶出は、経時的に塩濃度を上げる条件です。
イオン交換モードでは、分析種の荷電数が大きいほど、または水和イオン半径が小さいほど官能基との親和性が高くため、基本的に荷電数が小さい、または水和イオン半径が大きい分析種の順番に溶出します。
イオン交換クロマトグラフィーで用いる官能基を表3に示します。
(表3)イオン交換クロマトグラフィーで用いる官能基
| 分離モード | 陰イオン交換モード | 陽イオン交換モード | ||
|---|---|---|---|---|
| 官能基タイプ (イオン交換樹脂) |
強陰イオン交換基 (強塩基性イオン交換樹脂) |
弱陰イオン交換基 (弱塩基性イオン交換樹脂) |
強陽イオン交換基 (強酸性イオン交換樹脂) |
弱陽イオン交換基 (弱酸性イオン交換樹脂) |
| 代表的な官能基 | 第4級アンモニウム基 (QA) |
ジエチルアミノエチル基 (DEAE) |
スルホプロピル基 (SP) |
カルボキシルメチル基 (CM) |
| 対象試料 | 陰イオン性物質 | 陽イオン性物質 | ||
溶離液のpHは分析種や官能基の解離状態に影響を与えます。強イオン交換基は溶離液のpHによらず解離するので分析種の解離状態のみを考慮すれば良いですが、弱イオン交換基ではpHによって解離状態が変わるため官能基と分析種両者の解離状態を考慮する必要があります。
11-2. タンパク質分析
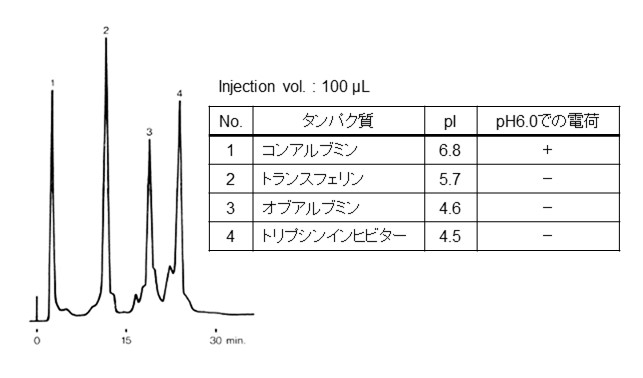
タンパク質は様々なアミノ酸がアミド結合した物質で、図19のように構造内に陽イオンや陰イオンが存在する両性イオンの物質です。このような両性イオンの物質の分析では特に注意が必要です。タンパク質は等電点 (pI)よりも低いpHの溶液中では正の電荷を帯び、高いpHの溶液中では負の電荷を帯びるため、分析に使用する溶離液のpHによって使用するイオン交換モード用カラムが異なってきます。
複数のタンパク質を分離する際は、pIの違いを考慮してカラムを選択することが重要です。
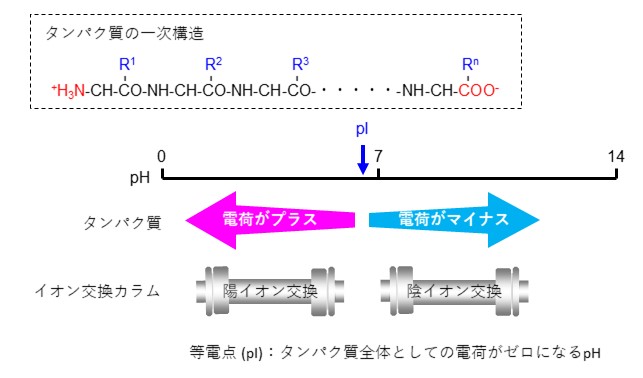
図20に強陰イオンモード(官能基:第4級アンモニウム基)を用いた標準タンパク質の溶出順序を示します。pH6.0の溶離液中では、コンアルブミンは正の電荷を、それ以外のタンパク質は負の電荷を帯びています。コンアルブミンは官能基と同じ陽イオンであるため、充てん剤には保持されずに最初に溶出します。その他のタンパク質はpIが低いものほど解離が大きく(負の電荷が大きく)なるため保持が強くなっています。
- Column
- :Shodex IEC QA-825 (8.0 mm I.D. x 75 mm)
- Eluent
- :(A); 20 mM Piperazine-HCl buffer (pH6.0)
(B); (A) + 0.5 M NaCl
Linear gradient; 0 min to 30 min, 100 % (A) to 50 % (B) - Flow rate
- :1.0 mL/min
- Detector
- :UV (280 nm)
- Column tamp.
- :Room temp.
イオン交換モード用の充てん剤にもポリマー基材とシリカ基材がありますが、溶離液にアルカリ溶媒を使用することもあるため、逆相モード用カラムのようにシリカ基材が圧倒的に多いわけではなく、ポリマー基材の割合が高くなっています。Shodexのイオン交換モード用カラムは、すべてポリマー基材を採用し、陰イオン交換モード、陽イオン交換モードそれぞれに対応したカラムをラインアップしています。
Shodexの陰イオン交換モード用カラムはこちら
Shodexの陽イオン交換モード用カラムはこちら
11-3. イオンクロマトグラフィーの分離機構
イオン交換モードの中で主に無機イオン、ハロゲン酸化物、アミン類、有機酸などを分析種としているのが、イオンクロマトグラフィーです。イオンクロマトグラフィーでは低イオン交換容量のカラムで分離し、電気伝導度検出器を用いるのが一般的です。カラムと電気伝導度検出器の間にサプレッサーという装置を配置し、カラムから溶出した溶離液をサプレッサーに通してから電気伝導度検出器に導入するサプレッサー法とカラムから溶出した溶離液をそのまま電気伝導度検出器に導入するノンサプレッサー法があります。電気伝導度検出器については「第5部:検出器」で説明します。
イオン交換モードと同様、溶出順序は基本的に荷電数が小さい、または水和イオン半径が大きい分析種の順番に溶出します。図21に無機陰イオン、図22に無機陽イオンの分析例を紹介します。
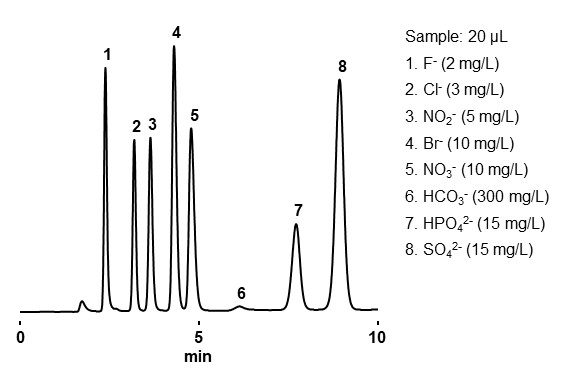
- Column
- :Shodex IC SI-90 4E (4.0 mm I.D. x 250 mm)
- Eluent
- : 1.8 mM Na2CO3 + 1.7 mM NaHCO3 aq.
- Flow rate
- :1.5 mL/min
- Detector
- :Suppressed conductivity
- Column tamp.
- :30 ℃
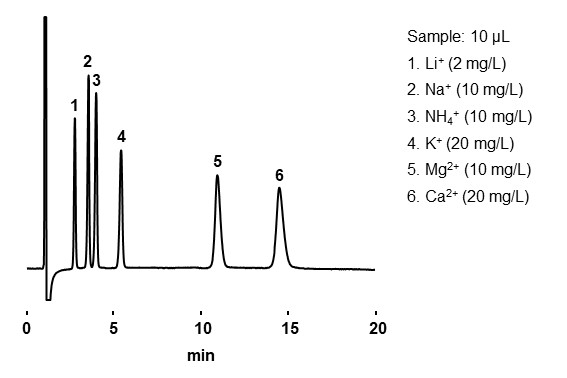
- Column
- :Shodex IC YS-50 (4.6 mm I.D. x 125 mm)
- Eluent
- :4 mM Methanesulfonic acid aq.
- Flow rate
- :1.0 mL/min
- Detector
- :Non-suppressed conductivity
- Column tamp.
- :40 ℃
Shodexでは、サプレッサー法、ノンサプレッサー法に対応した陰イオン分析用カラムおよび陽イオン分析用カラムをラインアップしています。
Shodexの陰イオン分析用カラムはこちら
Shodexの陽イオン分析用カラムはこちら
11-4. イオン排除モード(イオン排除クロマトグラフィー)の分離機構
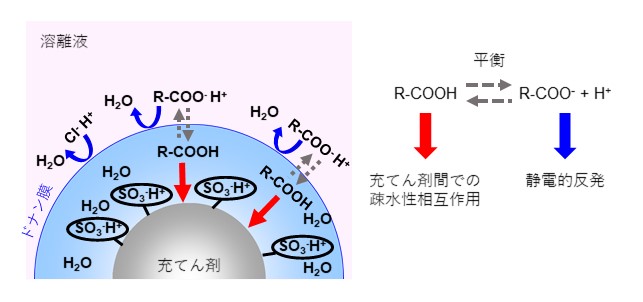
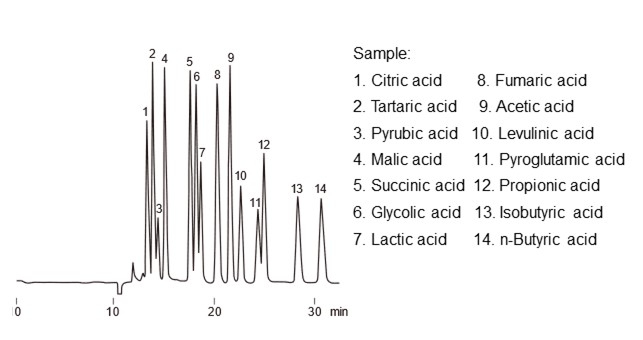
イオン交換モードがイオンの引きつけ合う力を利用するのに対し、イオン排除モードはイオンが反発し合う力(静電的反発)を利用した分離モードになります。イオン排除モードを用いた代表的な分析は有機酸の分析です。有機酸分析を例にイオン排除モードの分離機構を説明します。有機酸分析では、スルホ基のようなH型の強酸性イオン交換基を結合した充てん剤を用い、溶離液には過塩素酸や硫酸などの強酸性水溶液を用います。図23に示すようにイオン排除モードの分離機構はドナン膜を用いて説明されています。官能基と溶離液の境界部分にはドナン膜という仮想の膜が存在し、この膜を介して分配されるという考え方です。塩化物イオンや硫酸イオンなど強酸性のイオンは溶離液中でも完全に解離して陰イオンになります。このため官能基との静電的反発が大きくドナン膜を通過できず、充てん剤には保持されることなくカラムの中を通過します。一方、有機酸のような弱酸は、溶離液中で解離と非解離が平衡状態で存在します。非解離の有機酸はドナン膜を通過(膜内に分配)しますが、解離して陰イオンとなった状態では静電的反発を受けてドナン膜を通過することができません。このため、「電荷が大きい」すなわち「pKa(解離定数)が小さい」有機酸ほどドナン膜を通過しづらくなり早く溶出します。また、ドナン膜を通過した有機酸は充てん剤の基材との間で疎水性相互作用も生じるため、極性の低い有機酸ほど溶出が遅くなる傾向があります。図24にはイオン排除モードによる有機酸の分析例を示します。Shodexの有機酸分析用カラムは、スチレンジニビルベンゼン共重合体の基材に官能基としてスルホ基(H型)を結合させています。
- Column
- :Shodex RSpak KC-811 (8.0 mm I.D. x 300 mm) x 2
- Eluent
- :
6 mM HClO4 aq. - Flow rate
- :1.0 mL/min
- Detector
- :VIS (430 nm) *Post column method
- Column tamp.
- :50 ℃
Shodexのイオン排除モード用カラム(有機酸分析用カラム)はこちら
イオン交換モード、イオンクロマトグラフィー、イオン排除モードの比較は表4を参照ください。
(表4)イオン交換モード、イオンクロマトグラフィー、イオン排除モードの比較
| 分離モード | イオン交換モード | イオンクロマトグラフィー | イオン排除モード |
|---|---|---|---|
| 官能基 | 高交換容量のイオン交換基 | 低交換容量のイオン交換基 | 強酸性イオン交換基(H型) |
| 相互作用 | 静電的相互作用 | 静電的反発、疎水性相互作用 | |
| 分析種の溶出順序 | 荷電数が小さい順に溶出 水和イオン半径が大きい順に溶出 |
pKaが小さい順に溶出 極性が低い順に溶出 |
|
| 対象試料 | タンパク質、ペプチド、核酸など | 無機イオン、ハロゲン酸化物、アミン類、有機酸など | 主に有機酸 |
