12. 利用配位体交换能力差异分离
12-1. 什么是配位体
配位体即络合物中和中心的金属离子结合的分子或离子的总称。HPLC中所提到的配位体交换能力即官能团的对离子(金属离子)和糖的羟基之间形成络合物能力的强弱(配位能力)。
12-2. 配位体交换模式(配位体交换色谱法)的分离原理
利用配位体交换能力强弱进行分离的配位体交换模式主要用于糖的分析。众所周知,糖类是含有大量羟基的醛(醛糖)或酮(酮糖),具有能量稳定的椅型构象的环状结构。与各碳结合的羟基根据其键合位置呈水平 (equatorial位)或垂直 (equatorial位),根据糖的种类不同羟基的立体构造也各有差异。配位体交换模式使用的填料键合磺基官能团,这些磺基键合了金属离子作为对离子(抗衡离子)。金属离子和糖的羟基形成络合物,根据羟基立体构造的不同形成络合物的强弱也各有差异。配位体交换模式的分离原理如图25所示。(a)的立体构造有3个羟基和金属离子形成络合物 (triplet),(b)的立体构造只有2个羟基和金属离子形成络合物 (pair),形成的络合物比(a)中的弱。在配位体交换模式中,络合物形成能力越弱越早被洗脱。
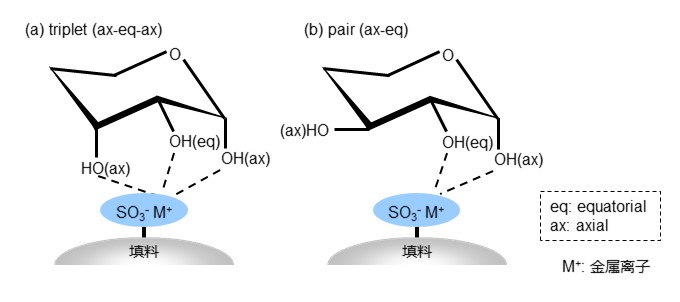
実在实际的糖分析中,利用的不仅仅是配位体交换模式,还会结合尺寸排阻模式(见下文)和上文介绍的HILIC模式进行分离。因此,即使配位能力没有差异,但如果分子大小和极性不同,也可以进行分离;反之,即使单独使用尺寸排阻模式或 HILIC 模式无法进行分离,也可以结合配体交换模式进行分离。图 26 显示了结合使用配体交换模式和尺寸排阻模式进行分析时糖类的洗脱顺序。由于采用了尺寸排阻模式,糖类按分子量大小依次洗脱,但葡萄糖(5号峰)和半乳糖(6号峰)是单糖和立体异构体。它们分子量相同,仅仅利用尺寸排阻模式无法分离,组合配位体交换模式后,可以分离开。
配位体交换模式利用这种配位能力的差异,适用于单糖类和二糖类的异构体的分离。
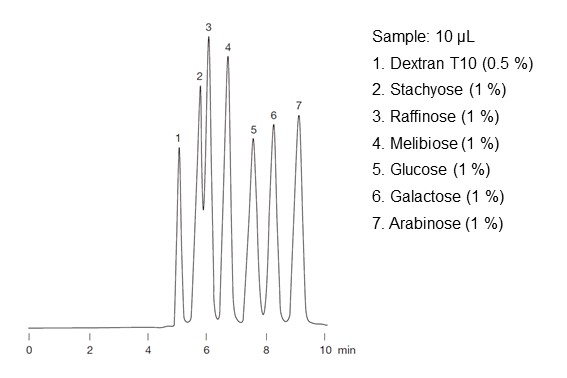
- Column
- :Shodex SUGAR SC1011 (8.0 mm I.D. x 300 mm)
- Eluent
- :H2O
- Flow rate
- :1.0 mL/min
- Detector
- :RI
- Column tamp.
- :80 ℃
配体交换模式中可以使用各种金属离子,络合物形成能力根据金属离子的种类而有所不同。对离子的络合物形成能力的强度的顺序大致如下。
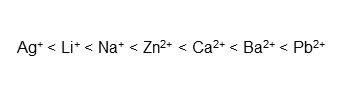
Shodex配备有键合了钙离子 (Ca2+)、铅离子 (Pb2+)、锌离子 (Zn2+)、钠离子 (Na+)的配位体交换色谱柱。
Shodex配位体交换和尺寸排阻模式相结合的色谱柱点击这里
Shodex配位体交换和HILIC模式相结合的色谱柱点击这里
可分离的糖类组合取决于选择的色谱柱。具体请参考各色谱柱的“糖的保留体积”页面。
13. 利用分子尺寸(分子量)差异分离
前面介绍的分离模式都是利用填料和分析物之间的相互作用来分离的。下面介绍的尺寸排阻模式则不是相互作用,而是利用物理性质(分子尺寸)进行分离。
13-1. 尺寸排阻模式(尺寸排阻色谱法)的命名
尺寸排阻色谱法 (Size exclusion chromatography; SEC)始于1955年美国的G. H. Lathe和C. R. J. Ruthven的发明。后来,瑞典的J.Porath和P.Flodin于1959年发表了一篇关于使用交联葡聚糖颗粒分离和脱盐蛋白质的论文,并在论文中将该技术命名为凝胶过滤色谱法 (Gel filtration chromatography; GFC)。1964 年,美国的J. C. Moore 发表了一种利用聚苯乙烯 (PS)颗粒测定合成聚合物分子量分布的方法,并将其命名为凝胶渗透色谱法 (Gel permeation chromatography; GPC)。从那时起,根据使用的流动相不同分别使用GFC和GPC来称呼,近年来科学术语统一为SEC,使用水溶液作为流动相的被称为水溶性SEC,使用有机溶剂作为流动相的被称为油溶性SEC。
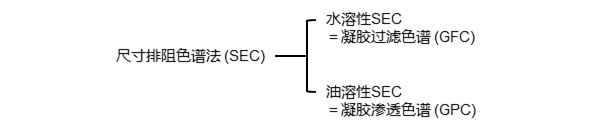
13-2. 尺寸排阻 (SEC)模式的分离原理
填料上有很多小孔, SEC模式色谱柱就是利用这些小孔来分离分析物。把小孔看作圆锥形来介绍SEC模式的分离原理。如图28中(a)所示,孔隙越深,直径越窄,因此分子尺寸较小的被分析物(蓝色)可以进入孔隙的深处,但随着被分析物分子尺寸的增大,它只能进入孔隙的一半(紫色,绿色),而随着分子尺寸的进一步增大,它根本无法进入小孔,只能通过填充物的表面,最快被色谱柱洗脱(橙色、粉色)。能进入小孔的分析物在通过色谱柱时会反复进出小孔,因此,能更深地进入小孔的小分子分析物在色谱柱中的移动距离更长。 此外,由于 SEC 模式是基于不存在其他相互作用,因此每种分析物的移动速度是恒定的,如图 28(b) 所示,在 SEC 模式中,分析物按照分子尺寸由大到小的顺序依次洗脱。
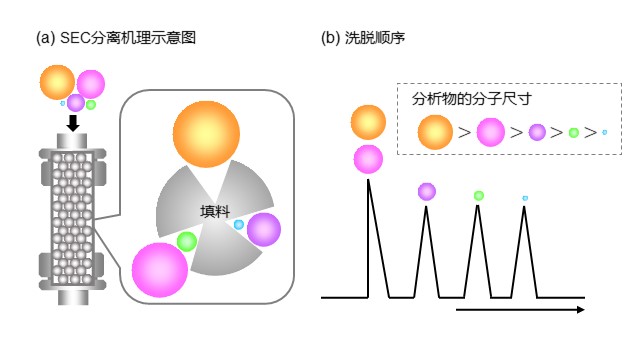
图29和图30分别是SEC 模式下分离标准蛋白质和聚碳酸酯的实例。对于蛋白质这类单分散(由单一分子量构成)的分析物,每种物质都会出一个峰。而合成高分子和多糖等具有分子量分布的聚合体,虽然会显示为单峰,但SEC模式也是按照分子大小顺序将它们洗脱出来从而形成单峰。
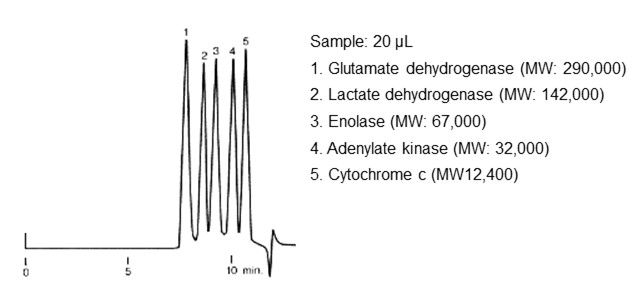
- Column
- :Shodex PROTEIN KW-803 (8.0 mm I.D. x 300 mm)
- Eluent
- :
50 mM Phosphate buffer (pH7.0) + 0.3 M NaCl - Flow rate
- :1.0 mL/min
- Detector
- :UV (280 nm)
- Column tamp.
- :Room temp.
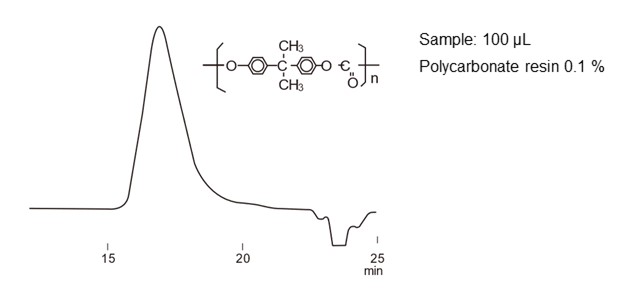
- Column
- :Shodex GPC KF-806L (8.0 mm I.D. x 300 mm) x 2
- Eluent
- :
THF - Flow rate
- :1.0 mL/min
- Detector
- :RI
- Column tamp.
- :40 ℃
13-3. 分子量测定
测定分子量和分子量分布对于了解聚合物的物理性质非常重要。SEC 模式通常用于测定聚合物的分子量和分子量分布,分析结果可提供诸如数均分子量 (Mn)、重均分子量 (Mw)和多分散性 (Mw/Mn)等信息。
在使用 SEC 模式进行分子量分布测定时,在与被分析物相同的分析条件下对已知分子量的标准样品进行分析,并绘制出称为标准曲线的曲线图,该曲线图显示了每个标准样品的分子量与峰顶保留时间(保留能力)之间的关系。这个标准曲线用于将聚合物峰的洗脱位置转换为分子量。
值得注意的是,SEC 模式是一种利用分子大小差异进行分离的模式。分子量相同但分子结构不同的聚合物不一定具有相同的分子尺寸。由于即使分子量相同,不同的分子大小在不同的位置洗脱,因此有必要使用与待测大分子结构相同的标准样品。但实际上很难为每种大分子制备标准样品,需要选择分子结构和溶解性与大分子相似的市售标准样品来制作标准曲线。所以从标准曲线中获得的分子量信息就是所用标准样品的分子量,即 "相对分子量"。
Shodex配有水溶性SEC用标准品普鲁兰、油溶性SEC用标准品聚苯乙烯 (PS)和聚甲基丙烯酸甲酯 (PMMA)。
Shodex的水溶性SEC (GFC)用标准品点这里
Shodex的油溶性SEC (GPC)用标准品点这里
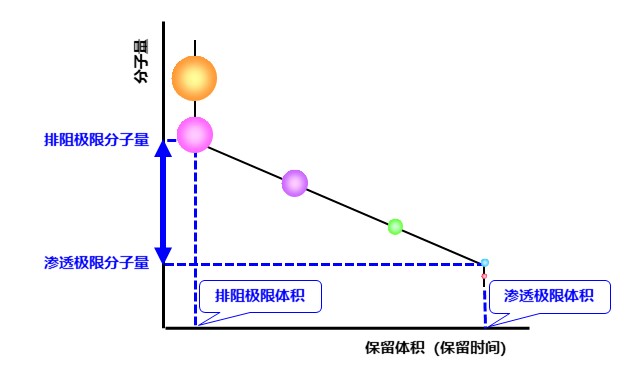
标准曲线的模型图如图 31 所示。如前所述,未进入小孔的大分子(橙色、粉色),即使它们的分子量(分子大小)不同,也会一起洗脱。在此位置洗脱的聚合物无法通过分子大小的差异进行分离。这个洗脱位置被称为“排阻极限”,在这个位置被洗脱的高分子中最小分子量被称为“排阻极限分子量”。而所有小于特定分子大小的被分析物质会深入孔隙,最后一起洗脱出来,导致无法分离。这个洗脱位置被称为 "渗透极限",在这个位置洗脱的大分子的最大分子量被称为 "渗透极限分子量"。
在测量聚合物的分子量分布时,重要的是要选择一种聚合物成分不会影响排阻极限(渗透极限)的色谱柱。
Shodex有各种孔径的色谱柱可用于SEC模式。
色谱柱的排阻极限分子量和适用于SEC分析的分子量范围等参考值已经列于网站和产品目录中,请在选择色谱柱时参考。
Shodex水溶性SEC(GFC)色谱柱点这里
Shodex油溶性SEC(GPC)色谱柱点这里
Shodex还配有主要利用SEC模式,根据流动相的选择配合反相模式、HILIC模式或离子交换模式的复合模式色谱柱,也有水/油两用型SEC色谱柱。
Shodex复合模式、水/油两用型SEC色谱柱点这里
14. 利用特异性差异分离
有些分离模式利用了样品本身的特异性。以下介绍手性分离和亲和色谱法。
14-1. 手性分离
手性异构体(对映体)是立体异构体的一种,其对称结构像照镜子一样相互映照。把这种无法重合的关系想象成一只左手和一只右手,就很容易理解了。其中一种手性异构体在光线照射下具有向右旋转的特性(右旋性),而另一种手性异构体则具有向左旋转的特性(左旋性),因此手性异构体也被称为光学异构体。尽管光学异构体的物理和化学性质完全相同,但被人体摄入后可能会产生不同的影响(生理活性)。例如,L-谷氨酸钠是众所周知的增鲜剂,而光学异构体D-谷氨酸钠几乎没有味道,也不能增鲜。类似这样的情况,其中一种可能显示出有用的生理活性,而另一种则没有,有时甚至对人体有害。有些制药原料具有光学活性。在生产过程中合成光学活性物质时,很难只合成所需的光学活性物质,光学异构体往往会同时合成,因此光学异构体的分离非常重要。光学异构体的色谱分离被称为手性分离。
用于手性分离的相互作用有多种类型,Shodex的手性分离色谱柱使用环状寡糖β-环糊精的衍生物作为配体的host-guest型色谱柱。分析物进入到β-环糊精的空隙中形成包接络合物并利用光学异构体的包合物络合能力差异来分离光学异构体。
Shodex的手性分离色谱柱点这里
14-2. 亲和色谱法
ア亲和色谱法的分离原理可以被喻为钥匙和钥匙孔之间的关系。与填料结合的配体被视为钥匙孔,而分析物则被视为钥匙,就像只有相配的钥匙才能打开钥匙孔一样,只有与配体具有生化亲和力的特定分析物才会被保留下来,其他成分都不会被保留。洗脱分析物时,通过改变流动相的组成使其和配体解离。因此,亲和色谱法具有高度选择性,是分离和生成分析物的绝佳分析技术,但必须为每种分析物设定配体、保留条件和解离条件。
