9. 分离模式的种类
在选择HPLC用色谱柱时,如果样品中的分析物种类很少且几乎没有杂质,则分析物能从色谱柱中洗脱即可,选择范围很广。但是如果样品中含有多种分析物或杂质,则必须选择一种不仅能让分析物从色谱柱中被洗脱,而且还能将各种分析物、杂质相互分离的色谱柱。选择色谱柱的第一步,是确认使用哪种分离模式。正如“5. 分离原理”中说明的那样,“相互作用的程度不同即可分离”,也可以理解为“如果利用被分析物与杂质之间的性质差异,即可分离”。表1总结了每种分离模式所使用的不同性质。
(表1)分离模式中使用的每种成分的不同性质
| 分离模式 | 性质差异 |
|---|---|
| 反相、正相、亲水性相互作用 (HILIC) | 极性 |
| 离子交换、离子排阻 | 离子性 |
| 配位体交换 | 配位体交换性 |
| 尺寸排阻 (SEC) | 分子大小(分子量) |
| 手性、亲和 | 特异性 |
| 复合模式 | 性质差异的组合 |
下面介绍各种分离模式的分离原理。
10. 利用极性差异分离
首先介绍下利用极性差异的分离模式。物质的极性可以表述为高极性、低极性,也可以表述为亲水性和疏水性。亲水性表示易溶于水,疏水性表示难溶于水。高极性=高亲水性,低极性=高疏水性。
10-1. 反相模式(反相色谱法)的分离原理
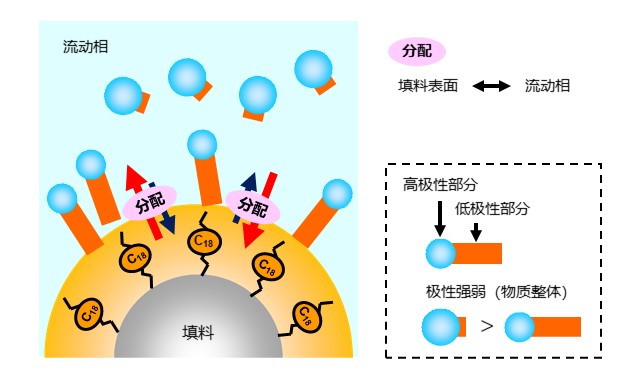
反相模式是一种利用被分析物极性差异进行分离的模式,也是最常用的分离模式,80% 以上的HPLC都采用反相模式。在反相模式中,使用极性低的填料和极性高的溶剂(如水/乙腈、水/甲醇等混合物)。分析物分布在 "填料极性"<"流动相极性"的环境中。因此,分析物的极性越强,就越向流动相方靠拢,即在色谱柱中移动速度变快,从而被较早洗脱。而极性较弱的分析物由于向填料方靠拢,从色谱柱中洗脱的时间较晚。因此,在反相模式下,被分析物基本按照极性从高到低的顺序洗脱。
图14显示了反相模式的分离原理,图15显示了反相模式下烷基醇的洗脱顺序。可以看出,烷基链(红字)越大的醇类的洗脱速度越慢。
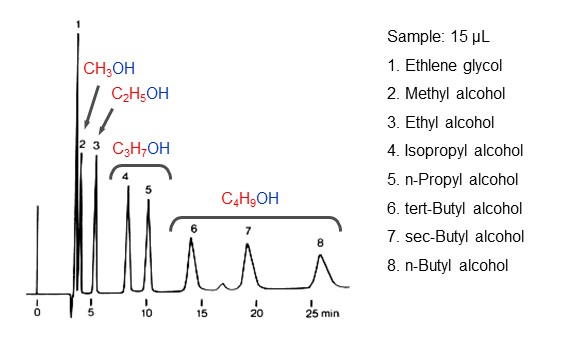
- Column
- : Shodex RSpak DE-613 (6.0 mm I.D. x 150 mm)
- Eluent
- :H2O
- Flow rate
- :1.0 mL/min
- Detector
- :RI
- Column tamp.
- :60 ℃
ODS色谱柱
ODS 色谱柱是典型的反相模式色谱柱。如下图所示,这种色谱柱的填料是在硅胶基质上键合了具有18个碳原子的直链烷基(十八烷基)官能团。当十八烷基键合到硅胶基质上时,使十八烷基硅烷化合物和硅胶基质表面的硅醇基发生反应(硅化),这种键合了十八烷基 (Octadecyl)的色谱柱就被命名为ODS色谱柱。ODS色谱柱在硅胶基质色谱柱中占比最大,可以说是HPLC中最常用的色谱柱。
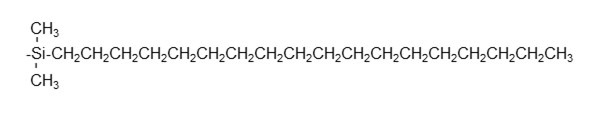
封端
当官能团键合到硅胶基质上时,并非所有硅醇基团都能和官能团结合,有些基团没有硅化残留下来了。这些未反应的硅醇基被称为残留硅醇基。根据分析物种的不同,残留硅醇基可能会引起意外的二次相互作用,从而影响分离效果。通常情况下,残留的硅醇基会经过二次硅烷化处理,即端封处理,以防止发生二次相互作用,但即使进行了端封处理,也很难使硅醇基完全硅化。即使使用的是ODS色谱柱,分析结果也会因色谱柱的不同而不同,原因之一就是残留的硅醇基。以下省略详细说明,ODS色谱柱有单体和聚合结合模式,结合模式的差异也会改变分离特性。
其他硅胶基质反相色谱柱
虽然ODS色谱柱是最常用的反相色谱柱,但如果十八烷基 (C18)对分析物的保留能力过强,可以通过改用碳数较少的直链烷基官能团来降低保留能力,如下所示。
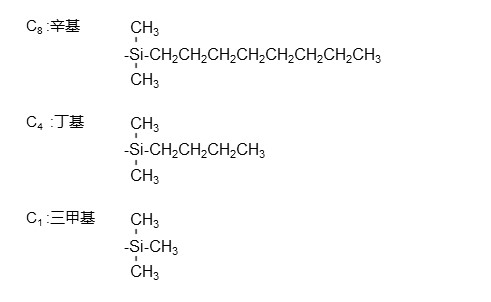
此外也有键合了苯基或氰丙基的其他反相色谱柱。
聚合物基质反相色谱柱
即使用聚合物基质作为填料的反相色谱柱。聚合物基质反相色谱柱的特长如下。
- (1)耐久性
硅胶基质的填料在保管和使用过程中会发生水解,造成键合相脱落的情况。而聚合物基质的化学稳定性高,被认为色谱柱的耐久性高。 - (2)再现性
硅胶基质填料很难对每个生产批次进行质量控制,而聚合物基质填料与硅胶基质相比,更容易控制生产过程并保持稳定的质量。
参考:RSpak DE系列的特长 (4) (批号再现性) - (3)耐碱性
硅胶基质一般被认为耐碱性较低。在分析碱性化合物时,有时会使用碱性流动相,因此具有高耐碱性的聚合物基质填料非常有效。当填料上吸附了杂质,造成色谱柱性能降低的时候,使用碱性溶剂清洗可能会有效果。当硅胶基质色谱柱无法进行碱性清洗必须更换色谱柱时,聚合物基质色谱柱可能通过碱清洗再生。
参考:聚合物基质反相色谱柱ODP-50 4E在碱性条件下的再现性
ODP2 HP的特长 (5) 耐碱性 - (4)分离性能一般来说,聚合物色谱柱的分离性能略逊于硅胶色谱柱,但聚合物色谱柱的性能也在日益提高。
Shodex以其长期积累的聚合物合成技术为基础,开发了一系列聚合物反相色谱柱。其中最常用的是Asahipak ODP系列。ODP这个名称指的是在聚合物(Polymer)基质(聚乙烯醇)填料上键合十八烷基(Octadecyl),熟悉ODS色谱柱用户应该很容易理解。
Shodex基于聚合物基质的反相色谱柱有多种产品,这些产品利用聚合物基质本身低极性,不键合官能团,仅仅使用基质本身作为填料。每种产品填料表面的极性和孔径有所不同。
10-2. 正相模式(正相色谱法)的分离原理
下面介绍正相模式。正相模式和反相模式一样,利用分析物极性的差异进行分离。正相模式使用高极性的填料(如硅胶等)和非极性流动相(如正己烷和异丙醇的混合溶液)。分析物在“填料表面极性”>“流动相极性”的环境下发生吸附(分配)作用。与反相模式相反,极性较低的分析物在色谱柱中移动较快,因此在正相模式中,基本上按照极性从低到高的顺序洗脱。
10-3. HILIC模式(亲水性相互作用法)的分离原理
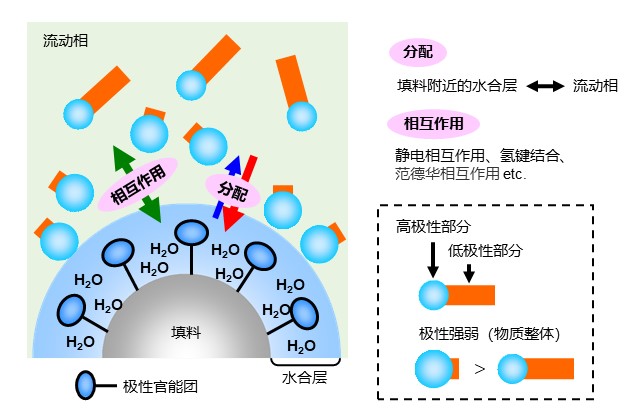
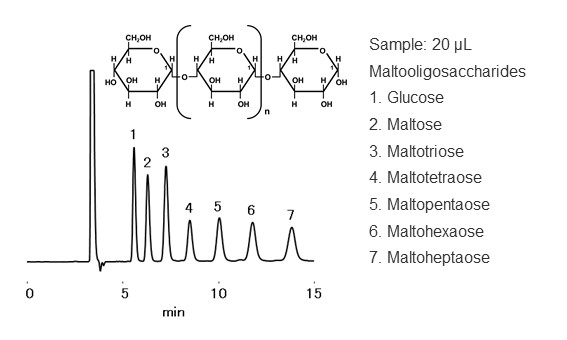
HILIC是亲水性相互作用法 (Hydrophilic Interaction liquid Chromatography)的简称。由美国的A. J. Alpert在1990年提出。HILIC模式从广义上讲属于正相模式,其历史背景是早在 1990 年之前就已作为正相模式使用,例如用于糖分析。HILIC模式使用在硅胶基质或聚合物基质上键合酰胺基、氨基或二醇基官能团的表面极性高的填料。虽然和反相模式相同,流动相使用水和乙腈混合溶液等高极性溶剂,但HILIC模式使用的流动相中有机溶剂的比例很高。在这种环境下,填料表面会形成水合层,分析物在“填料表面极性”>“流动相极性”的环境下进行分配作用,按照极性从高到低的顺序被洗脱。HILIC模式的流动相和反相模式相似,但洗脱顺序与反相模式相反。HILIC模式除了分配之外,还通过静电作用、氢键作用和范德华相互作用共同发挥作用。HILIC模式的分离原理如图16所示,低聚麦芽糖在HPLIC模式下的洗脱顺序如图17所示。低聚麦芽糖是由葡萄糖与α-1,4葡萄糖苷键合而成的寡糖。葡萄糖的结构中有多个羟基 (OH基),结合的葡萄糖越多,极性就越大。糖链较大的寡糖洗脱速度较慢。
- Column
- :Shodex HILICpak VG-50 4E (4.6 mm I.D. x 250 mm)
- Eluent
- :CH3CN/H2O=65/35
- Flow rate
- :0.7 mL/min
- Detector
- :RI
- Column tamp.
- :40 ℃
HILIC模式可以分析在反相模式下保留能力较弱或难以保留的高极性化合物。利用这一特点,HILIC模式可以用于分析包括糖在内的各种高极性化合物。Shodex除了提供在聚合物基质上键合了氨基的Asahipak NH2P系列色谱柱,还有在聚合物基质填料上键合各种官能团的HILICpak系列色谱柱。这些HILIC模式色谱柱和聚合物基质反相色谱柱相同,具有很高的化学稳定性和出色的耐碱性。
表2总结了反相模式、正相模式和HILIC模式的比较。
(表2)反相模式、正相模式、HILIC模式的比较
| 分离模式 | 反相模式 | 正相模式 | HILIC模式 |
|---|---|---|---|
| 填料表面 | 低极性 | 高极性 | 高极性 |
| 流动相 | 高极性 | 低极性 | 高极性 |
| 分析物的洗脱顺序 | 极性从高到低 | 极性从低到高 | 极性从低到高 |
| 对象样品 | 药物、表面活性剂、肽、水溶性维生素等 | 脂肪酸、磷脂、脂溶性维生素等 | 糖、寡核酸、氨基酸、肽、药物代谢物等 |
| 特征 | ・主要以低分子(分子量小于2,000)为对象 ・适用于多种样品 |
・主要以低分子(分子量小于2,000)为对象 ・适用于在反相中保留过强的化合物 ・立体结构识别能力强,适用于异构体分离 ・流动相去除容易,易于制备和浓缩。 |
・主要以低分子(分子量小于2,000)为对象 ・适用于反相模式中难以保留的高极性化合物 ・适用于高极性化合物的LC/MS微量分析(高灵敏度分析) |
Shodex的反相模式色谱柱、HILIC模式色谱柱请点击这里
11. 利用离子性差异分离
就像磁铁的N极和S极相互吸引一样,带正电的"阳离子"和带负电的"阴离子"相互吸引。而与磁铁的N极之间、S 极之间相互排斥一样,阳离子之间、阴离子之间相互排斥。离子物质包括如蛋白质、肽、氨基酸和儿茶酚胺等生物物质,如有机酸等有机物及如氯离子 (Cl-)和钠离子 (Na+)等无机离子。以下将介绍利用离子间吸引力(静电相互作用)的离子交换模式和利用离子间排斥力(静电排斥)的离子排阻模式。
11-1. 离子交换模式(离子交换色谱法)的分离原理
以下以分析物为阴离子为例,介绍离子交换模式的分离原理。
分析物为阴离子物质时,使用阳离子官能团作为键合相的填料。离子交换模式一般使用缓冲液或盐的水溶液作为流动相。
- 流动相中的阴离子通过静电相互作用吸附在键合相的阳离子上。当流动相持续通过色谱柱时,流动相中的阴离子之间互相竞争,反复吸附解吸附并在色谱柱内移动。(图18的(1))
- 分析物(阴离子物质)进入色谱柱中后和色谱柱中本来已经吸附的流动相中的阴离子互相竞争,吸附在键合相上。(图18的(2)、(3))
- 分析物和流动相中的阴离子互相竞争的同时(反复吸附解吸附)在色谱柱内移动。(图18的(4)、(5))
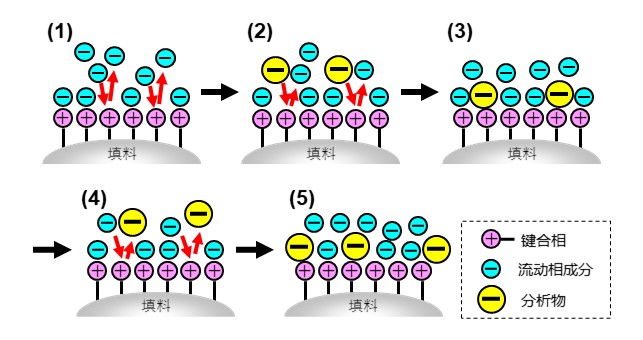
分析物和流动相中的竞争离子交换的同时在色谱柱中移动,因此分析物的保留会随着流动相离子强度增加而减弱。离子交换模式中,经常使用随时间改变流动相组成的“梯度洗脱”来更快地洗脱保留较强的分析物。经典的梯度洗脱是随时间增加盐浓度。
在离子交换模式下,被分析物的电荷数越多或水合离子半径越小,对官能团的亲和力就越高。基本上是按照电荷数由少到多,或者水合半径由大到小的顺序洗脱。
离子交换模式中使用的键合相如表3所示。
(表3)离子交换模式使用的官能团
| 分离模式 | 阴离子交换模式 | 阳离子交换模式 | ||
|---|---|---|---|---|
| 键合相种类 (离子交换树脂) |
强阴离子交换基团 (强碱性离子交换树脂) |
弱阴离子交换基团 (弱碱性离子交换树脂) |
强阳离子交换基团 (强酸性离子交换树脂) |
弱阳离子交换基团 (弱酸性离子交换树脂) |
| 典型键合相 | 季铵基 (QA) | 二乙基氨基乙基 (DEAE) | 磺基丙基 (SP) | 羧基甲基 (CM) |
| 对象样品 | 阴离子性物质 | 阳离子性物质 | ||
流动相的pH会影响分析物和键合相的解离状态。强离子交换基的解离不受流动相pH的影响,因此只需要考虑被分析物的解离状态,而对于弱离子交换基团,其解离状态会随pH值的变化而变化,因此必须同时考虑键合相和被分析物的解离状态。
11-2. 蛋白质的分析
蛋白质是结合了各种各样氨基酸、酰胺的物质,如图19所示,其结构是阳离子和阴离子共存的两性离子物质。分析这类两性离子物质需要特别注意。蛋白质在pH值低于其等电点 (pI)的溶液中带正电,而在pH值较高的溶液中带负电,因此所使用的离子交换模式色谱柱取决于分析所用流动相的pH值。
分析多种蛋白质样品时,考虑pI的不同来选择合适的色谱柱非常重要。
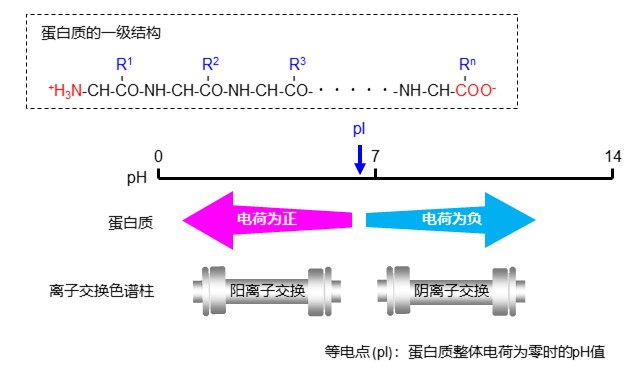
图20显示了采用强阴离子模式(键合相:季铵基)的标准蛋白质的洗脱顺序。在pH6.0的流动相中,伴清蛋白带正电荷,其他的蛋白质带负电荷。伴清蛋白和官能团同为阳离子,所以无法被填料保留,最快被洗脱出来。其他的蛋白质由于pI越低解离度越高(带负电荷较多),所以保留能力越强。
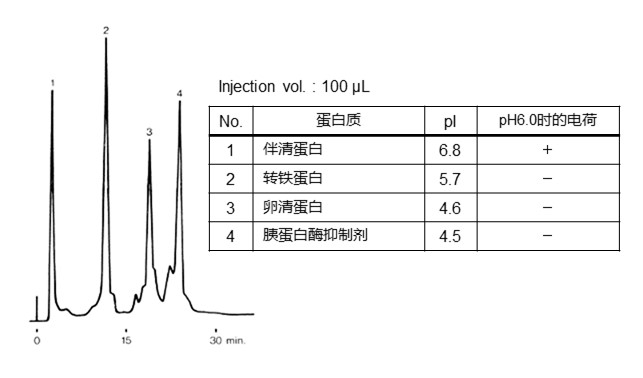
- Column
- :Shodex IEC QA-825 (8.0 mm I.D. x 75 mm)
- Eluent
- :(A); 20 mM Piperazine-HCl buffer (pH6.0)
(B); (A) + 0.5 M NaCl
Linear gradient; 0 min to 30 min, 100 % (A) to 50 % (B) - Flow rate
- :1.0 mL/min
- Detector
- :UV (280 nm)
- Column tamp.
- :Room temp.
离子交换模式的填料也有聚合物和硅胶两种基质,但由于流动相有时使用碱性溶剂,所以不像反相模式色谱柱那样硅胶基质占主导地位,聚合物基质色谱柱的占比很高。Shodex的离子交换色谱柱都采用聚合物基质,阴离子交换模式、阳离子交换模式都有各种色谱柱可供选择。
Shodex阴离子交换色谱柱点击这里
Shodex阳离子交换色谱柱点击这里
11-3. 离子色谱法的分离原理
离子交换模式中,主要分析无机离子、卤氧化物、胺和有机酸等样品的称为离子色谱法。离子色谱法使用低离子交换容量的色谱柱进行分离,通常使用电导检测器。色谱柱和电导检测器之间连接一个称为抑制器的装置,分为流动相从色谱柱中洗脱出来通过抑制器后进入电导检测器的抑制器法以及流动相从色谱柱中洗脱出来直接进入电导检测器的非抑制器法两种。电导检测器将在第4部分进行说明。
和离子交换模式相同,基本上按照电荷数由少到多或者水合离子半径由大到小的顺序洗脱。图21是无机阴离子,图22是无机阳离子的分析实例。
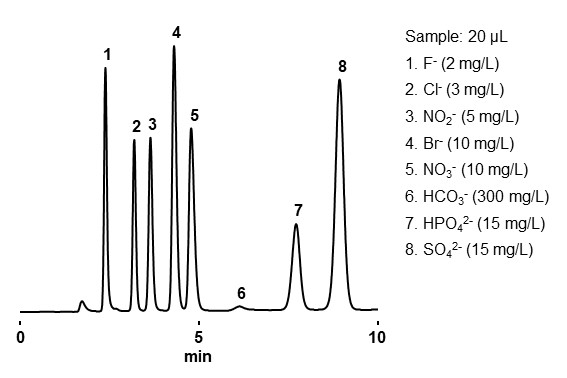
- Column
- :Shodex IC SI-90 4E (4.0 mm I.D. x 250 mm)
- Eluent
- : 1.8 mM Na2CO3 + 1.7 mM NaHCO3 aq.
- Flow rate
- :1.5 mL/min
- Detector
- :Suppressed conductivity
- Column tamp.
- :30 ℃
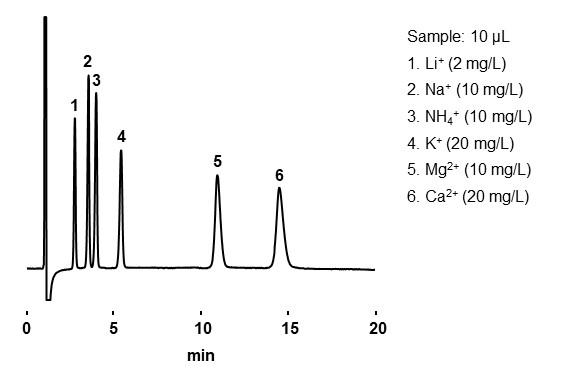
- Column
- :Shodex IC YS-50 (4.6 mm I.D. x 125 mm)
- Eluent
- :4 mM Methanesulfonic acid aq.
- Flow rate
- :1.0 mL/min
- Detector
- :Non-suppressed conductivity
- Column tamp.
- :40 ℃
Shodex配备抑制器法、非抑制器法对应的阴离子分析色谱柱以及阳离子分析色谱柱。
Shodex阴离子分析色谱柱点击这里
Shodex阳离子分析色谱柱点击这里
11-4. 离子排阻模式(离子排阻色谱法)的分离原理
离子交换模式利用的是离子之间的吸引力,而离子排阻模式则是利用离子之间的排斥(静电排斥)进行分离的模式。使用离子排阻模式进行的经典分析是有机酸分析。下面以有机酸分析为例,解释离子排阻模式的分离原理。在有机酸分析中,使用带有H型强酸性离子交换基团(如磺基)的填料,并使用强酸性水溶液(如高氯酸或硫酸)作为流动相。如图23所示,使用道南膜来介绍离子排阻模式的分离原理。在官能团和流动相之间存在一个虚拟膜,即道南膜,通过这个膜进行分配。氯离子和硫酸根离子等强酸性离子在流动相中即可完全解离形成阴离子。因此和官能团的静电排斥很大无法通过道南膜,无法被填料保留,直接从色谱柱中通过。而有机酸等弱酸,在流动相中处于解离和非解离的平衡状态。非解离的有机酸可以通过道南膜(膜内分配),但是解离成阴离子状态的部分因为受到静电排斥无法通过道南膜。因此,“带有高电荷”即“pKa(解离系数)小”的有机酸更难通过道南膜,洗脱速度更快。此外,通过道南膜的有机酸还有可能和填料的基质产生疏水性相互作用,有机酸的极性越低,洗脱速度越慢。图24是离子排阻模式分析有机酸的应用实例。Shodex的有机酸分析色谱柱使用苯乙烯-二乙烯基苯共聚物作为填料基质,键合相为磺基 (H型)。
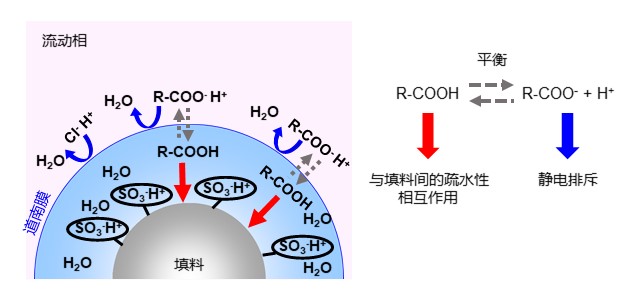
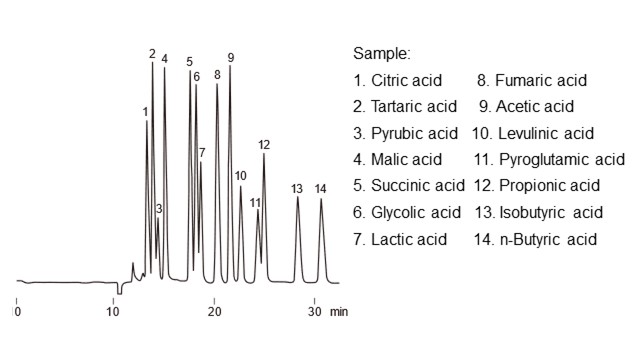
- Column
- :Shodex RSpak KC-811 (8.0 mm I.D. x 300 mm) x 2
- Eluent
- :
6 mM HClO4 aq. - Flow rate
- :1.0 mL/min
- Detector
- :VIS (430 nm) *Post column method
- Column tamp.
- :50 ℃
Shodex离子排阻色谱柱(有机酸分析色谱柱)点击这里
离子交换模式、离子色谱法、离子排阻模式的比较请参考表4。
(表4)离子交换模式、离子色谱法、离子排阻模式的比较
| 分离模式 | 离子交换模式 | 离子色谱法 | 离子排阻模式 |
|---|---|---|---|
| 键合相 | 高交换容量的离子交换基 | 低交换容量的离子交换基 | 强酸性离子交换基 (H型) |
| 相互作用 | 静电相互作用 | 静电排斥、疏水性相互作用 | |
| 分析物的洗脱顺序 | 电荷数从低到高 水合离子半径从大到小 |
pKa从小到大 极性从低到高 |
|
| 对象样品 | 蛋白质、肽、核酸等 | 无机离子、卤氧化物、胺、有机酸等 | 主要为有机酸 |
